Les cliniciens du VIH ont émis une mise en garde concernant le cabotégravir et la rilpivirine injectables à action prolongée dans un récent commentaire sur le SIDA. Le Dr Diego Ripamonti de l’hôpital Papa Giovanni XXIII de Bergame et ses collègues des universités de Milan et de Sienne soulignent que les personnes ayant un long historique de traitement en particulier pourraient ne pas être de bons candidats au traitement, en raison du risque important de développer une résistance aux médicaments. le traitement échoue.
Le traitement anti-VIH injectable à longue durée d’action par le cabotégravir et la rilpivirine change la donne dans le monde du traitement du VIH, car il s’agit de la toute première association de médicaments anti-VIH qui n’a pas besoin d’être prise quotidiennement. Ils offrent de l’espoir à ceux qui ont du mal à prendre leurs pilules chaque jour et au rappel quotidien de leur séropositivité qui en découle, ou à ceux qui se sentent obligés de cacher leurs pilules aux autres.
Dans les essais cliniques, le cabotégravir et la rilpivirine injectables se sont révélés tout aussi efficaces que les pilules quotidiennes pour supprimer le VIH à des niveaux indétectables. Par exemple, l’essai SOLAR a comparé des injections de cabotégravir à action prolongée et de rilpivirine tous les 2 mois avec un régime oral quotidien standard. Un an plus tard, 403/447 (90 %) des personnes recevant des injections et 207/223 (93 %) des personnes recevant un régime oral avaient une charge virale inférieure à 50.
Cependant, chez la petite minorité de participants pour lesquels le traitement injectable n’a pas fonctionné (environ 1 % (26/2 313) des participants aux cinq essais cliniques principaux), il y avait un taux élevé de résistance émergente aux inhibiteurs de l’intégrase (la classe de médicaments auquel appartient le cabotégravir) et les INNTI (classe médicamenteuse de la rilpivirine). La résistance à ces types de médicaments (en particulier les inhibiteurs de l’intégrase) constitue un gros problème pour les patients, car elle limite considérablement les types de traitement anti-VIH qui supprimeront efficacement leur VIH.
Les auteurs soulignent que même si la prise de pilules 80 à 85 % du temps est suffisante pour éviter l’échec du traitement avec la plupart des traitements anti-VIH modernes, certains de ceux qui ont développé une résistance aux médicaments injectables au cabotégravir et à la rilpivirine au cours des essais ont eu une parfaite observance.
Ils soulignent également que le niveau de résistance émergente dans les essais sur le cabotégravir et la rilpivirine injectables est plus élevé que tout autre schéma thérapeutique « simplifié » (c’est-à-dire un traitement associant moins de médicaments que le schéma thérapeutique triple standard), même en incluant le dolutégravir en monothérapie – un schéma thérapeutique qui a été critiqué par de nombreux experts et son utilisation n’est pas recommandée. Alors, qu’est-ce que cela signifie pour ceux qui envisagent de passer au traitement injectable par le cabotegravir et la rilpivirine ?
Comprendre les données sur la résistance aux médicaments
Nous explorons ici plus en détail les données sur l’échec du traitement et la résistance aux médicaments issues des essais cliniques sur le cabotégravir et la rilpivirine injectables. Le premier tableau ci-dessous (Tableau 1) présente les taux d’échec virologique confirmé et de résistance émergente parmi les participants aux cinq essais cliniques randomisés sur le cabotegravir et la rilpivirine injectables.
ATLAS et FLAIR ont comparé l’efficacité des injections administrées toutes les 4 semaines avec des schémas thérapeutiques oraux. LATTE-2 a comparé l’efficacité d’injections administrées toutes les 4 semaines et toutes les 8 semaines avec un régime oral. ATLAS-2M a comparé l’efficacité d’injections administrées toutes les 4 semaines avec des injections administrées toutes les 8 semaines. SOLAR a comparé l’efficacité d’injections administrées toutes les 8 semaines avec un régime oral.
Dans les cinq études, l’échec virologique confirmé était défini comme lorsque deux tests de charge virale consécutifs détectaient une charge virale supérieure à 200 copies par ml chez une personne qui avait auparavant une charge virale supprimée. Le tableau comprend des données sur la « résistance émergente » – cela signifie que la résistance aux inhibiteurs de l’intégrase (comme le cabotégravir) ou aux INNTI (comme la rilpivirine) n’a pas été détectée dans les échantillons de sang prélevés avant que les participants ne commencent le traitement injectable et a été détectée dans les échantillons de sang après le début du traitement par les participants. traitement injectable. Dans cette situation, la résistance est liée au traitement plutôt qu’à une résistance préexistante causée par un traitement antérieur ou transmise lors de l’acquisition du VIH.
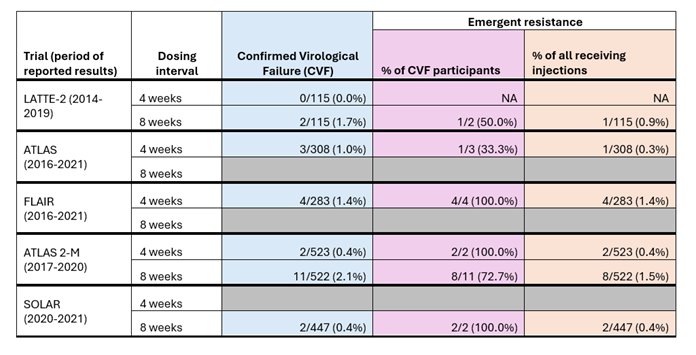
Le tableau montre que le nombre de personnes ayant connu un échec virologique confirmé (colonne en bleu) dans les cinq essais était très faible, allant de 0 à 2,1 %, avec un peu plus de personnes ayant reçu des injections toutes les 8 semaines ayant connu un échec virologique confirmé que celles ayant reçu des injections toutes les 8 semaines. reçu des injections toutes les 4 semaines. Parmi ceux avec un échec virologique confirmé (colonne en violet), les taux de résistance émergente étaient élevés, allant de 33,3 % à 100 %.
Tableau 1 : Échec virologique confirmé et taux de résistance émergente chez les participants recevant du cabotégravir et de la rilpivirine injectables dans cinq essais cliniques.
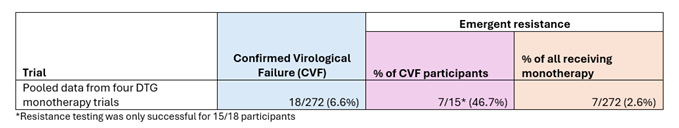
Le deuxième tableau (Tableau 2) montre les taux d’échec virologique confirmé et de résistance émergente parmi les participants à quatre essais cliniques randomisés sur le dolutégravir en monothérapie. Il ressort que le taux d’échec virologique confirmé était beaucoup plus élevé pour ce schéma médicamenteux que pour le traitement injectable, à 6,6 %. Mais le taux de résistance émergente parmi les patients présentant un échec virologique confirmé était inférieur, à 46,7 %, à celui de quatre des cinq essais sur le cabotegravir et la rilpivirine injectables.
Tableau 2 : Échec virologique confirmé et taux de résistance émergente parmi les participants aux essais sur le dolutégravir en monothérapie.
Cependant, si l’on considère le taux de résistance émergente parmi toutes les personnes recevant le médicament testé dans l’essai (la colonne en orange dans les tableaux 1 et 2), alors le risque de développer une résistance émergente à la suite d’une monothérapie au dolutégravir est beaucoup plus élevé, soit 2,6 % que tous les essais de traitement injectable (où la résistance émergente variait entre 0,3 % et 1,5 % selon la posologie). Ainsi, le risque absolu de développer une résistance émergente au cabotégravir et à la rilpivirine injectables est bien inférieur à celui du dolutégravir en monothérapie, mais le risque relatif parmi ceux qui connaissent un échec thérapeutique est plus élevé.
Comment les cliniciens peuvent-ils réduire le risque qu’une personne développe une résistance émergente ?
Depuis la publication des résultats des essais précédents, des recherches ont été menées sur les facteurs de risque susceptibles d’augmenter la susceptibilité d’une personne à développer une résistance aux médicaments lors de l’utilisation de cabotégravir et de rilpivirine injectables.
Une étude a regroupé les données d’ATLAS, FLAIR et ATLAS-2M et a révélé que trois facteurs augmentaient le risque d’échec du traitement. Il s’agissait des éléments suivants : avoir le sous-type A6/A1 du VIH-1 ; avoir un indice de masse corporelle (IMC) égal ou supérieur à 30 ; et avoir des mutations génétiques associées à une résistance à la rilpivirine avant de commencer le traitement. Cependant, ils ont constaté que la présence de l’un de ces facteurs ne suffisait pas à elle seule à augmenter le risque d’échec du traitement : ce n’était que lorsqu’une personne en présentait deux ou plus que son risque augmentait. De plus, toutes les personnes ayant connu un échec thérapeutique ne présentaient pas ces facteurs de risque, de sorte que la raison de l’échec de leur traitement reste inexpliquée.
En conséquence de ces résultats, les directives de prescription recommandent que les personnes présentant au moins deux de ces facteurs de risque ne se voient pas prescrire du cabotégravir et de la rilpivirine injectables. Ils recommandent également d’exclure toute personne présentant une résistance préexistante connue ou suspectée aux INNTI ou aux inhibiteurs de l’intégrase.
Cependant, Ripamonti et ses collègues soulignent qu’il peut être difficile pour les cliniciens d’établir ces informations, pour deux raisons.
Premièrement, les outils les plus couramment utilisés pour identifier les sous-types du VIH ne sont pas suffisamment spécifiques pour distinguer le sous-type A6 des autres sous-types A, et de nombreux laboratoires n’effectuent pas les tests appropriés pour identifier les mutations génétiques associées à la résistance à la rilpivirine. Notamment, 4 des 8 participants du groupe de traitement de 8 semaines de l’étude ATLAS-2M et 1 des 2 participants de l’étude SOLAR qui ont développé une résistance émergente ont ensuite été identifiés comme ayant également une résistance aux INNTI ou aux inhibiteurs de l’intégrase avant de commencer le traitement. étude, ce qui signifie que les essais cliniques avaient également initialement négligé ces facteurs de risque, même s’ils disposaient de plus de ressources que dans les soins de routine.
Deuxièmement, les personnes qui suivent un traitement anti-VIH depuis longtemps n’ont peut-être pas vu tous leurs échecs thérapeutiques identifiés et enregistrés à ce moment-là. Par exemple, les personnes qui suivaient un traitement il y a plus de 25 ans utilisaient probablement des médicaments présentant un risque beaucoup plus élevé de résistance émergente, à une époque où les tests de résistance et même les tests de charge virale n’étaient pas largement disponibles. Dans de nombreux pays, les cliniques ne testent pas régulièrement la résistance aux médicaments, même si un patient présente un échec virologique.
En conséquence, les auteurs formulent les recommandations suivantes :
- Les facteurs qui exposent les personnes à un risque de développer une résistance aux médicaments doivent être étudiés de manière approfondie avant de prescrire du cabotégravir et de la rilpivirine injectables. Les cliniciens devraient notamment s’efforcer d’utiliser les tests de résistance de l’ADN pour détecter les mutations archivées, bien que ce test ne soit pas toujours disponible.
- Les médecins doivent être prudents lorsqu’ils prescrivent du cabotegravir et de la rilpivirine injectables à action prolongée à des patients ayant des antécédents de traitement longs et/ou complexes. En outre, les personnes ayant un faible nombre de cellules CD4 ou ayant déjà souffert du SIDA ont été exclues des essais cliniques et pourraient également courir un risque d’échec du traitement.
- Avant de faire passer un patient au cabotégravir et à la rilpivirine injectables, les cliniciens doivent identifier de manière proactive les options de traitement restantes en cas d’échec du traitement et de développement d’une résistance aux deux médicaments.
Par rapport à leur dernière recommandation, les auteurs soulignent que dans la plupart des cas d’échec virologique, il serait conseillé d’inclure du darunavir boosté dans leur schéma thérapeutique adapté. Par conséquent, ils conseillent que les candidats au passage au cabotegravir et à la rilpivirine injectables ne devraient pas avoir connu auparavant de rebond viral sous inhibiteurs de protéase, même s’ils n’ont pas développé de résistance en conséquence. Les cliniciens doivent également rassembler toutes les informations disponibles sur les allergies ou intolérances antérieures au darunavir ou aux agents stimulants et sur le risque d’interactions médicamenteuses entre le darunavir boosté et tout autre médicament que prend le patient.
« Aussi attrayante que puisse paraître cette option à action prolongée, les cliniciens et les personnes vivant avec le VIH doivent être conscients des risques associés, en pesant soigneusement tous les facteurs de base et en planifiant la stratégie de sortie appropriée en cas d’échec », concluent le Dr Ripamonti et ses collègues.
Source : AidsMap