Un millilitre de sang contient environ 15 gouttes individuelles. Pour une personne atteinte du virus de l’immunodéficience humaine (VIH), chaque goutte de sang peut contenir de moins de 20 copies du virus à plus de 500 000 copies. Appelée la charge virale, c’est ce qui est mesuré pour permettre aux cliniciens de comprendre comment les patients réagissent aux médicaments antiviraux et de surveiller la progression potentielle.
Le test de la charge virale , qui prend beaucoup de temps, doit être répété plusieurs fois au cours du traitement d’un patient. Maintenant, une équipe de recherche de Penn State a développé un test numérique rapide et économique qui peut mesurer directement la présence du VIH dans une seule goutte de sang. Ils ont publié les travaux dans ACS Nano .
Selon l’auteur correspondant Weihua Guan, professeur agrégé de génie électrique et de génie biomédical au Penn State College of Engineering, le test numérique est la première étape pour fournir un outil de diagnostic clinique pour une multitude de maladies infectieuses.
Les tests conventionnels de la charge virale du VIH consistent à prélever du matériel génétique de l’échantillon, à l’amplifier et à le comparer à des échantillons de référence. Le test de référence, appelé RT-PCR, peut produire une estimation précise de la charge virale réelle, mais ce n’est pas une mesure directe. Guan et son équipe ont adopté une approche plus directe avec leur test, nommé Self-digitization Through Automated Membrane-based Partitioning (STAMP), qui est moins cher, plus rapide et nécessite moins de sang que la RT-PCR.
« Voici comment cela fonctionne : nous prélevons un petit échantillon du sang d’une personne et en extrayons l’ARN viral, le matériel génétique du virus », a déclaré Guan. « Nous mélangeons ensuite cet ARN avec une protéine spéciale appelée Cas13, qui fait partie du système CRISPR. »
CRISPR-Cas13 est un « outil révolutionnaire », a déclaré Guan, qui permet aux chercheurs de cibler et de manipuler des séquences d’ARN. Dans cette étude, les chercheurs exploitent la technologie non pas pour ses capacités d’édition, mais pour son potentiel de diagnostic. Ils utilisent CRISPR-Cas13 pour détecter et signaler la présence du VIH.
Une fois l’ARN combiné avec Cas13, les chercheurs placent une membrane en polycarbonate nanoporeux – un filtre fin facilement disponible, ce qui en fait un matériau rentable, a déclaré Guan – sur le mélange. Les nanopores sont si minuscules qu’ils peuvent diviser le mélange en gouttelettes uniques contenant une seule molécule d’ARN, à laquelle est attachée la protéine Cas13. Si le VIH se trouve dans la molécule d’ARN, la protéine Cas13, qui est activée par l’ARN du VIH, coupera les molécules rapporteuses, générant un signal que les chercheurs peuvent détecter.
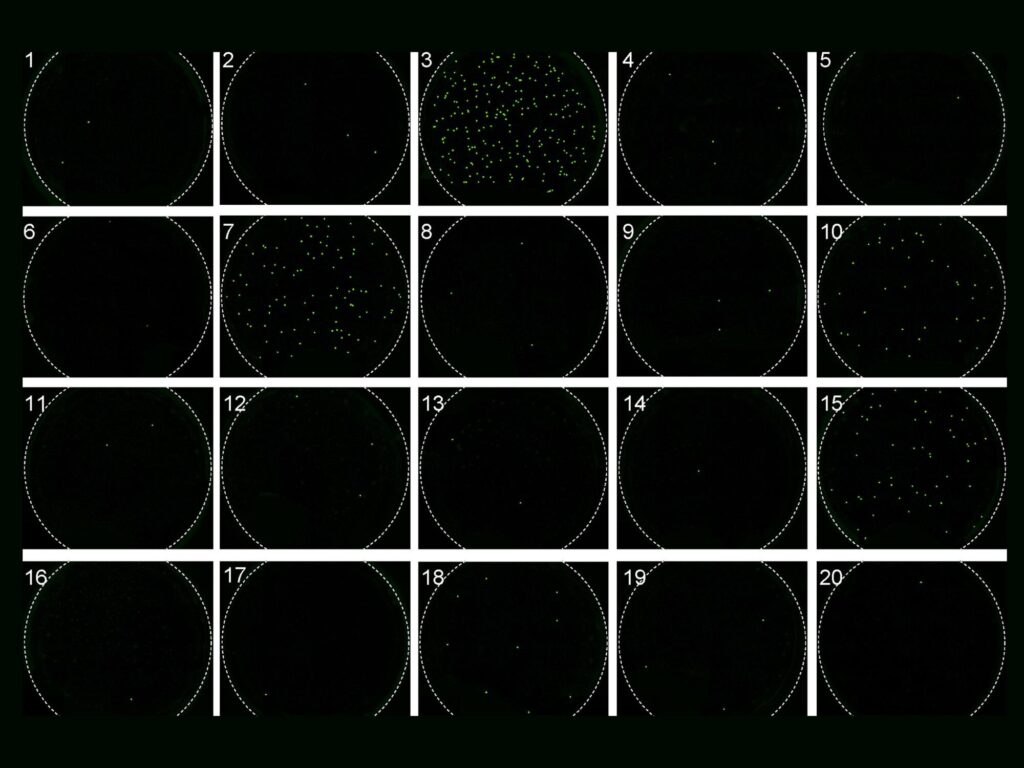
« En comptant le nombre de gouttelettes montrant ce signal, nous pouvons déterminer la quantité de VIH dans le sang de la personne », a déclaré Guan. « Plus il y a de gouttelettes avec le signal, plus la charge virale est élevée. »
Les chercheurs ont testé cette approche avec de l’ARN synthétique du VIH pour optimiser la sensibilité et la précision du test avant de tester le plasma de laboratoire et éventuellement les échantillons de plasma des patients. Ils ont validé la méthode STAMP en quantifiant les charges virales du VIH dans 20 échantillons de plasma de patients avec une précision comparable à la méthode RT-PCR traditionnelle, qui nécessite généralement plus de sang. Guan a déclaré qu’ils travaillaient à se procurer davantage d’échantillons pour poursuivre leurs tests.
L’équipe a également constaté que l’approche peut fournir une évaluation précise des charges virales du VIH égales ou supérieures à environ 2 000 copies de virus par millilitre de sang. Une charge virale est considérée comme faible lorsqu’il y a moins de 10 000 copies du virus par millilitre ; indétectable à 20 exemplaires ou moins; et élevé à environ 100 000 exemplaires mais peut s’étendre au-delà d’un million.
Selon Guan, la plage de détection de 2 000 à 10 000 peut être importante pour les cliniciens surveillant les patients pour un rebond viral. Les personnes sous traitement antirétroviral (ART) peuvent atteindre des niveaux de virus indétectables, ce qui signifie qu’elles ne peuvent plus transmettre sexuellement le virus, mais l’augmentation des niveaux de virus peut indiquer qu’un individu développe une résistance à l’ART ou un autre problème.
« Alors que d’autres améliorations sont nécessaires pour améliorer sa limite de détection et automatiser la configuration, la méthode CRISPR numérique basée sur STAMP montre un grand potentiel pour faire progresser la surveillance de la charge virale du VIH », a déclaré Guan, expliquant que les chercheurs prévoient de continuer à améliorer l’efficacité et la précision de la plateforme. pour quantifier plusieurs virus, dans le but ultime de commercialiser l’appareil.
Source : Médical X press